在之前的文章《外泌體如何申請INCI名稱》中,我們介紹了什麼是外泌體產品。外泌體是細胞外囊泡(extracellular vesicles, EVs)中的一個亞群,直徑約為20~200 nm(納米),包含了蛋白質、脂質、多醣及RNA等物質,通過作用於靶細胞,外泌體在細胞間信號轉導和訊息傳遞中發揮重要作用。
外泌體來源於多種細胞,不同細胞分泌的外泌體含有不同的生物學功能。具體來看,植物外泌體的研究相較動物和人體領域的研究較為有限。植物外泌體是植物細胞分泌的納米級小囊泡,直徑約為40~150nm,內含DNA、小RNA、微小RNA和蛋白質等物質,介導細胞間的信號轉導和訊息傳遞。
美國上市的外泌體原料
目前各個國家和地區對外泌體的監管一般都對人源外泌體和非人源外泌體進行區分式管理,整體來說,人源外泌體的管理更加嚴格。美國是目前沒有對外泌體提出專門管理規定的國家之一。那麼,在美國市場,目前有哪些外泌體原料上市了呢?
瑞歐通過兩個途徑進行收集,第一是美國個人護理品協會(PCPC)wINCI線上資料庫中已收錄的外泌體相關INCI名稱,第二是美國FDA藥品評價與研究中心(CDER)公布的DMF產品名。雖然不能完全覆蓋美國市場上的外泌體原料,但可以作為企業參考。
表1 PCPC線上資料庫中收錄的含“Exosomes”的INCI名稱(統計截至2025年2月)
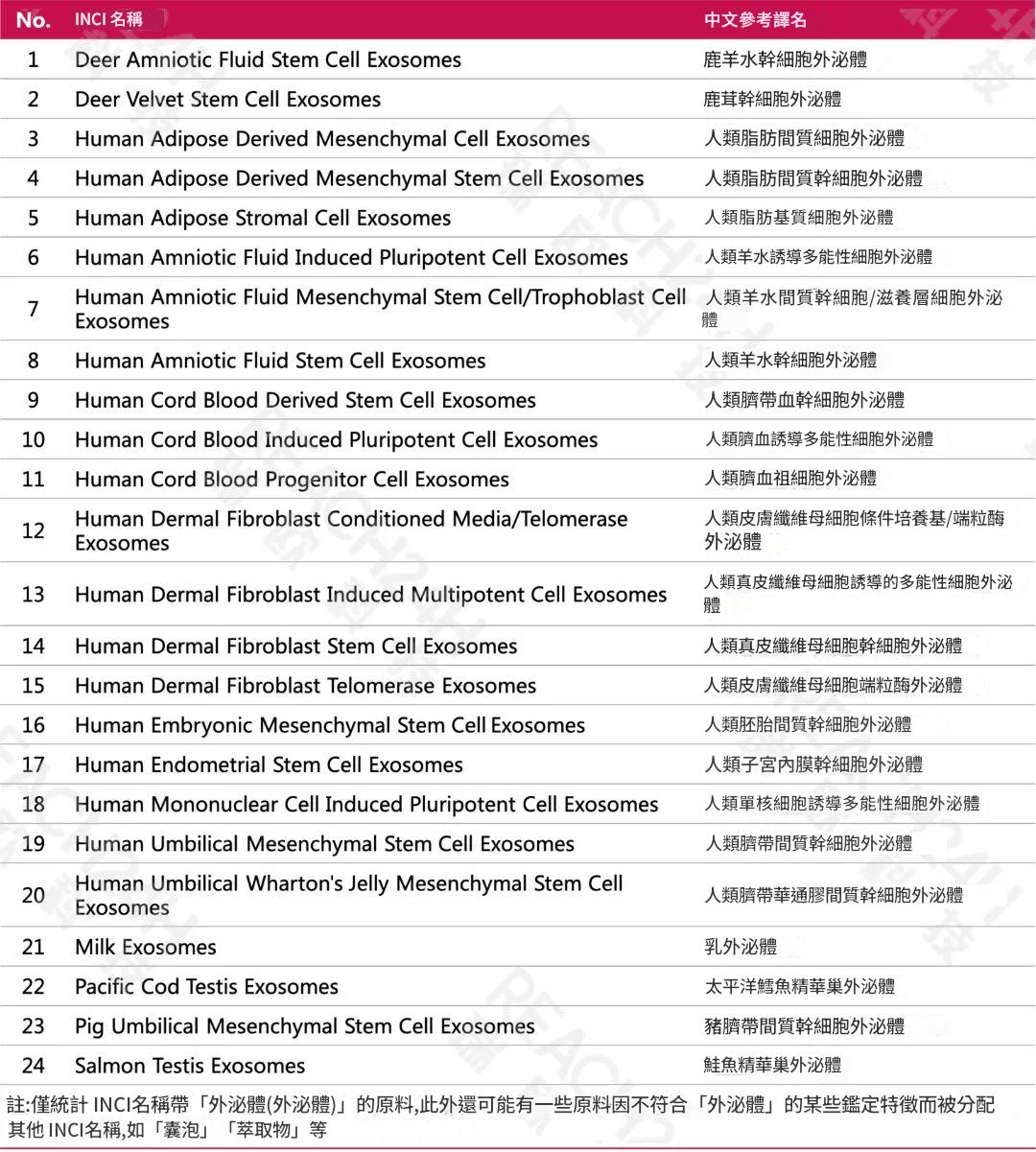
表2 CDER最新公布的DMF清單中帶“Exosomes”的產品(統計截至2025年2月)
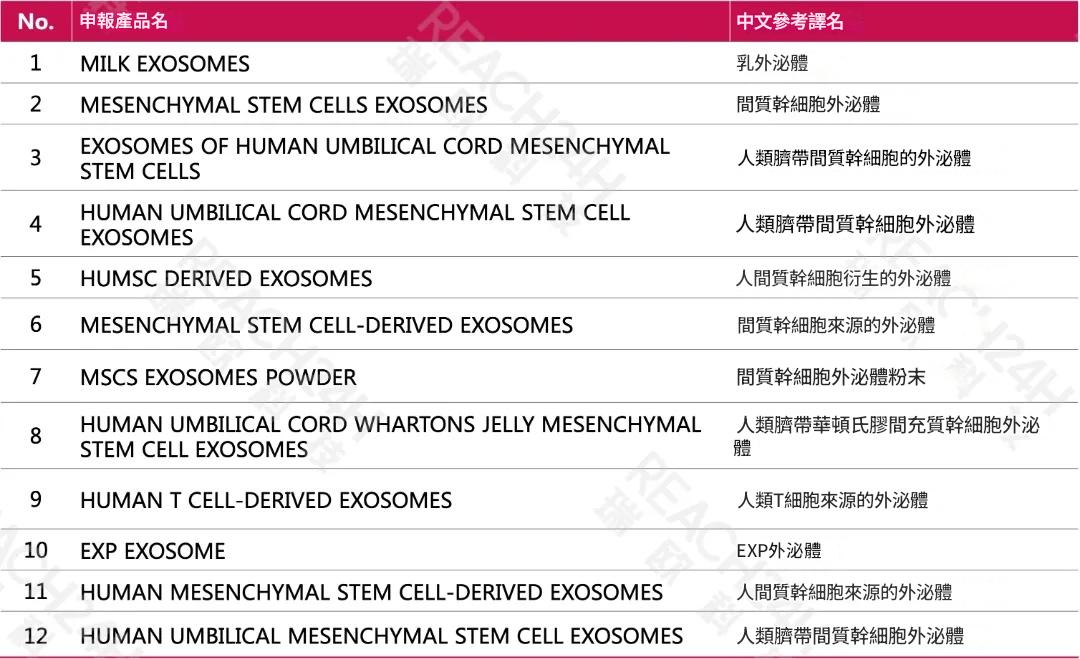
從上圖表格中可以發現,PCPC線上資料庫中已收錄的外泌體相關INCI名稱共24個。人源外泌體最多,其餘有鹿源外泌體、海洋生物源外泌體、牛奶外泌體等。CDER公布的DMF產品名中含外泌體的共有12個,大部分還是人源外泌體,比如各類間充質幹細胞外泌體有9個。
美國外泌體申請提示
雖然美國目前沒有對外泌體提出專門管理規定,但按照美國化妝品和藥品法規的原則,企業仍然是保證產品安全的責任主體,加上美國鼓勵消費者對於不安全/違反消費者知情權的產品進行群體訴訟,因此企業在將產品投放美國時仍需要把控產品品質,以免在事後監管時承擔高額的違規成本,比如可以考慮依據現有的申請渠道做好自身產品評估和資料整理。
外泌體INCI名稱申請一般需要提供以下資料:
商品名、成分說明、主要功能、來源細胞/組織、製程簡述、外泌體和來源細胞的鑑定資料、外泌體純度等。
外泌體DMF申請一般需要提供以下資料:
名稱、結構、製造商資訊、工藝控制資訊、物料控制資訊、雜質研究資訊、品質標準、驗證資訊、穩定性研究等。
而參考日本和韓國對於人源外泌體的要求,一般也會重視捐贈者的健康資訊、製程、細胞培養/生產過程中的品質管理、培養基成分、產品穩定性、病原細菌/病毒/血清測試等方面。
相關文章:

