GRAS(Generally Recognized As Safe),是美國食品藥物管理局(FDA)針對食品中,在正常使用條件下被專家普遍認定安全的物質所做的分類。 目前美國 GRAS 分成兩種形式:FDA GRAS通報和自我聲明GRAS。依據相關法規認定的GRAS物質,可以合法在美國市場進行銷售,且無需事前通報FDA或取得核准。
近日,美國FDA官網更新了GRAS通報名錄,瑞歐科技對最新公布的申報清單(GRN 1235-1257)進行了整理,並歸納出以下未來食品原料創新的核心趨勢,提供企業參考。
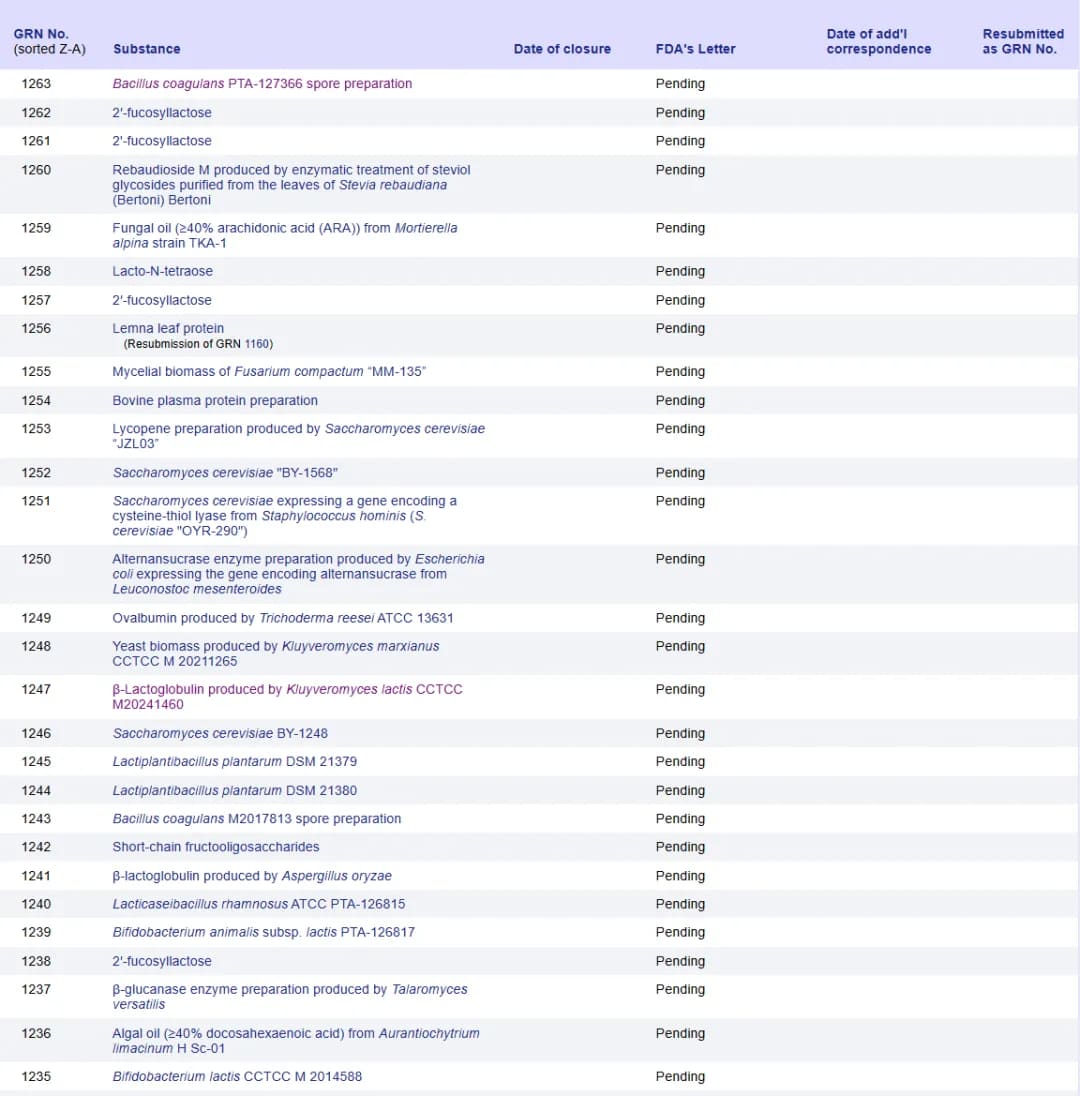 來源:hfpappexternal.fda.gov
來源:hfpappexternal.fda.gov
精準發酵與合成生物學成為新亮點
在這次更新的申報清單中,透過基因工程改造的微生物作為「細胞工廠」生產的無動物(Animal-free)蛋白格外受到關注。這股由合成生物學所帶動的浪潮,正從根本上重塑蛋白質的價值鏈,為功能性食品、植物基產品,甚至整個食品體系的永續發展,帶來顛覆性的解決方案。
GRN 1241&1247 β-乳球蛋白(β-Lactoglobulin):一種主要的乳清蛋白,分別由米曲霉(Aspergillus oryzae)和乳酸克魯維酵母(Kluyveromyces lactis)生產。
GRN 1249卵清蛋白(Ovalbumin):雞蛋清中的主要蛋白質,由里氏木黴(Trichoderma reesei)生產
GRN 1255緊湊鐮刀菌(Fusarium compactum)的菌絲體生物質:一種菌菇蛋白(Mycoprotein)
母乳寡糖成為美國GRAS申報清單中的矚目焦點
在這次更新清單中,5家企業均申報了母乳寡糖,其中4家企業申報2'-FL,顯示2'-FL已經成為炙手可熱的熱門原料。這種罕見的「集體申報」現象,清楚反映出背後龐大的市場需求,以及日益激烈的技術競爭。
作為母乳中的核心功能成分(HMO),2'-FL和LNT在嬰幼兒健康領域的重要作用已獲得業界普遍認同,因此成為高端嬰兒配方食品市場的「必爭之地」。而密集的申報更顯示微生物發酵技術日趨成熟,正推動這些明星成分從前沿概念快速邁向市場「標配」。
GRN 1238, 1257, 1261, 1262:2'-岩藻糖基乳糖(2'-FL)
GRN 1258:乳糖-N-四糖 (LNT)
益生菌研發持續火熱
腸道健康話題依舊高溫不退,益生菌的申報仍是熱門焦點。值得注意的是,益生菌市場已經走過「概念導向」階段,正式進入「菌株為王」的時代。各家企業申報的菌株愈來愈具體,對應的功能定位也更加明確。
GRN 1235:乳雙歧桿菌CCTCC M 2014588
GRN 1239:動物雙歧桿菌乳亞種PTA-126817
GRN 1240:鼠李糖乳桿菌ATCC PTA-126815
GRN 1243:凝結芽孢桿菌M2017813孢子製劑
GRN 1244&1245:植物乳桿菌DSM 21379&21380
美國FDA GRAS直被視為全球食品創新的權威風向標,這次的申報趨勢再度顯示,未來將由合成生物學與微生物製造技術所主導。因此,瑞歐科技也建議相關產業的業者,應及早展開 GRAS 佈局,以搶佔國際市場先機並建立核心競爭力。
如何進行美國GRAS認證申請
理論上,任何機構或個人均可以通過以下任一途徑申請美國GRAS認證。
1. 自我聲明GRAS(Self-affirmed GRAS)
由具備資格的專家團隊進行審查並簽署報告,形成 GRAS 評估資料,但不需向 FDA 通報,也不會公開相關資訊。
2. FDA GRAS (FDA notified GRAS)
將 GRAS 評估資料提交給 FDA,由其專家進行審查並給予正式回覆。需注意的是,FDA notified GRAS通常在送件時,也會包含自我聲明 GRAS 的專家意見與結論。
簡單來說:
自我聲明 GRAS → 可直接在美國市場銷售,但對外宣傳效果有限。
FDA GRAS → 更有利於市場推廣與品牌公信力,但審查週期較長。業者可依自身市場規劃選擇合適途徑。
相關文章:
最新整理!益生菌GRAS認證數量飆升,FDA GRAS成市場指標!
什麼是GRAS物質? 如何申請美國GRAS認證? 需要哪些必備資料?

