化妝品原料的安全評估是成品安全評估的基礎,本篇我們將詳細介紹,如何減少化妝品新原料中的動物測試,一起來看:
動物測試的替代需求,一方面,來自行業和消費者對於動物福利和“零殘忍”的關注日益提高,推動法規立法重視動物試驗的“減少(Reduction)、優化 (Refinement) 和替代 (Replacement)” 。
另一方面,也是安全評估方法和毒理測試方法快速發展進步的結果。越來越多的國家和地區在化妝品的安全評價方面提出要使用動物替代方法,包括歐盟、美國、加拿大、挪威、澳大利亞等。
中國的替代方法不斷擴充
《化妝品安全技術規範》收錄的替代方法正在不斷擴充:
2021年第31號公告《化妝品新原料註冊備案資料管理規定》(以下簡稱“規定”)中規定,有條件的接受動物替代方法。
化妝品新原料毒理學試驗項目應當按照《化妝品安全技術規範》規定的試驗方法開展。
目前,中國對化妝品新原料的申報資料要求仍以動物試驗數據為主,但一直在積極推動化妝品替代試驗研究與驗證體系的建設,越來越多的動物替代方法被收錄於《化妝品安全技術規範》。
在這裡,我們對其中的非動物測試方法進行了彙總。
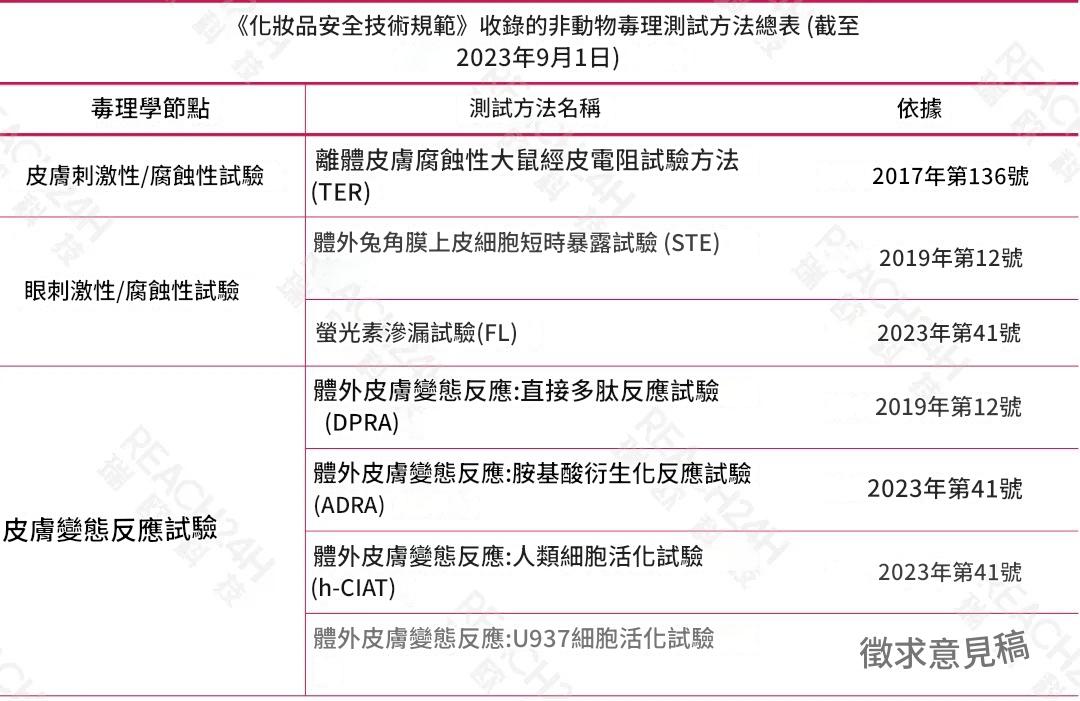

國際上的替代方法
《規定》要求應用的動物替代試驗方法尚未收錄於中國《化妝品安全技術規範》的,該項替代試驗方法應當為國際權威替代方法驗證機構已收錄的方法,且應當同時提交該方法能準確預測該毒理學終點的證明資料。
證明資料應當包括該項替代試驗方法研究過程簡述和不少於 10 種已知毒性受試物的研究數據、結果分析、研究結論等內容。
國際權威替代方法驗證機構主要包括:
經濟合作與發展組織(OECD)
國際化妝品監管合作組織(ICCR)
美國替代方法驗證跨部門協調委員會(ICCVAM)
歐盟動物試驗替代方法參考實驗室(EURL-ECVAM)
日本替代方法驗證中心(JaCVAM)
韓國替代方法驗證中心(KoCVAM)
加拿大衛生部(Health Canada)
...
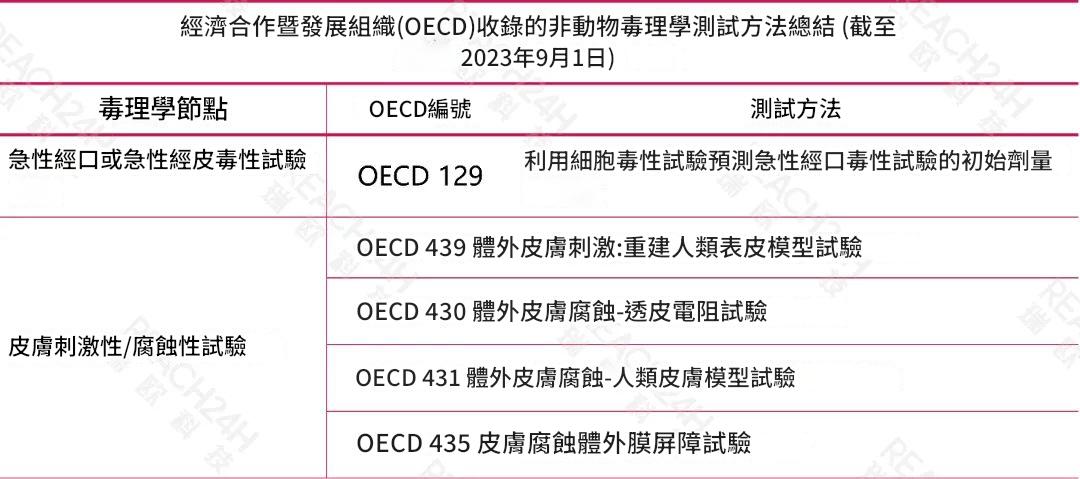
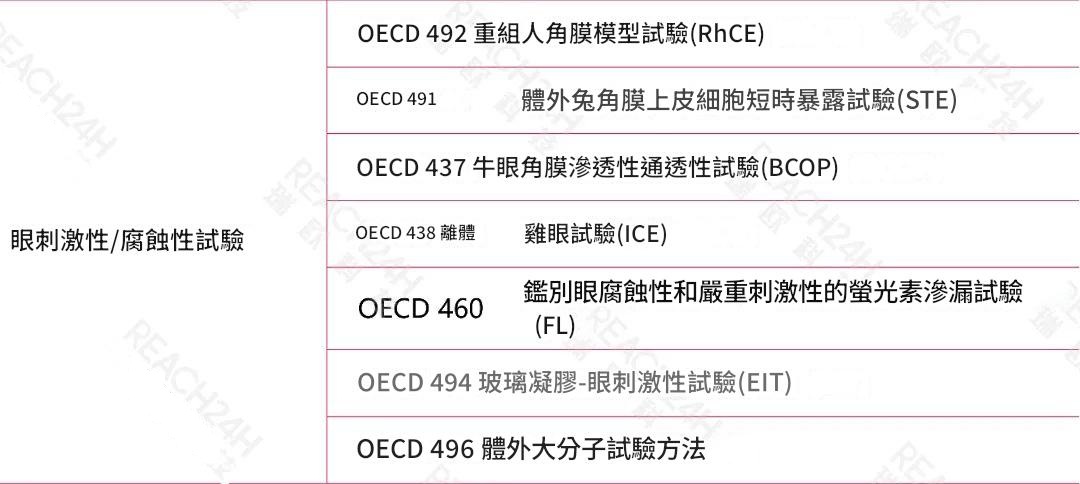
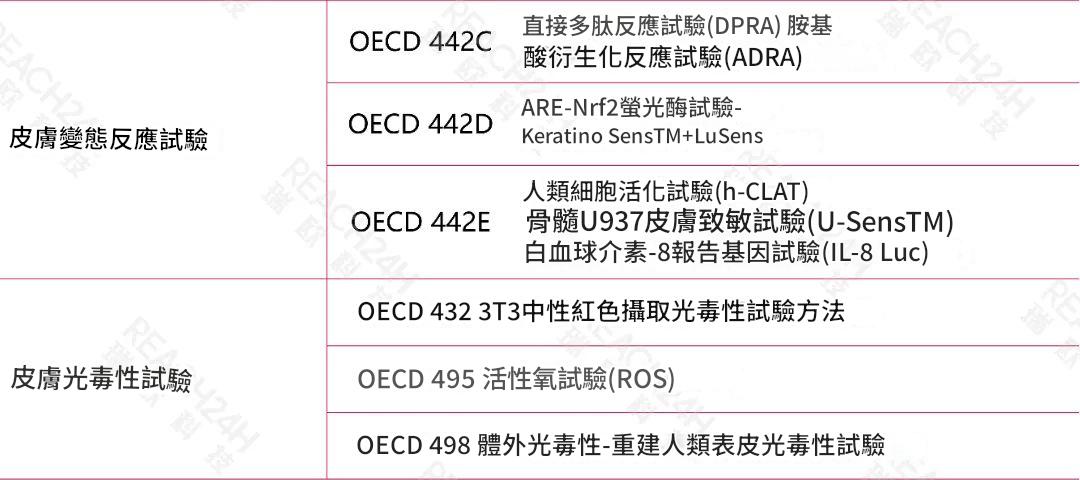

可豁免動物試驗的情形
什麼情形的化妝品新原料有可能不開展動物試驗完成申報?
對於化妝品新原料相關的毒理學試驗,皮膚光變態反應試驗國內外當前階段仍無非動物試驗替代方法。此外,關於系統毒性,仍存在缺乏有效的替代方法的問題。
3種情形
基於上述原因,對於化妝品新原料申報,僅有《規定》中的三種情形有可能不開展動物試驗完成申報:
情形6:聚合物情形原料。
情形5:具有安全食用歷史的原料,且原料不具有紫外吸收特性。
情形3:具有3年安全使用歷史的低風險原料,且原料不具有紫外吸收特性,同時具有國際權威安全評價機構評價結論認為在化妝品中使用是安全的安全評估報告,或符合倫理學條件下的人體安全性檢驗報告。
方法適用性
此外,需注意,非動物試驗替代方法均需結合方法的適用性,且大部分替代方法是細胞或者人造組織的測試,對於原料的組成和理化特性有要求,選擇方法時需要留意。
例如:
OECD 129:根據當前的研究,該測試僅能作為預測急性經口毒性的初始劑量的替代方法;
OECD 491 體外兔角膜上皮細胞短時暴露試驗 (STE):若受試物不能溶於或均勻混懸於生理鹽水、5% 的 DMSO / 生理鹽水溶液或礦物油時不適用;
OECD 442C 體外皮膚變態反應:直接多肽反應試驗,適用於單一組分(定量組成的物質,且其中一種主要成分含量至少 80%(W/W))化妝品用化學原料或已知組成成分的多組分(定量組成的物質,且其中一種以上成分含量大於等於 10%,小於 80%)化妝品用原料。
整合測試策略
同時,單一的替代方法可能存在不足,必要時應採用整合測試策略(ITS)組合不同方法進行全面評估。
《規定》要求在化妝品新原料的註冊備案過程中,使用動物替代方法進行毒理學安全性評價的,應當根據原料的結構特點、特定的毒理學終點選擇合適的整合測試和評估方法(IATA)評價新原料的毒性。
例如:
眼刺激性/腐蝕性評價:目前常用的整合策略為自下而上(Bottom-Up)及自上而下(Top-Down)策略。
OECD 467推薦了以BCOP為核心方法的組合策略,規定性方法1 (DAL-1) 為BCOP+RhCE,規定性方法2 (DAL-2) 為BCOP+STE。
皮膚致敏性評價:OECD 497推薦了3種評估策略,其中2o3策略是在導致皮膚致敏的3個關鍵事件中選取至少2個開展。
包括KE1:蛋白質結合(DPRA);KE2:角化細胞活化(KeratinoSens™);KE3:樹突狀細胞激活(h-CLAT),是無需專家判斷的方法。
以上就是對目前國內非動物測試方法的匯總,希望貫徹「零殘忍」產品測試策略的企業,可以關注國內替代試驗方法的更新進展,新測試方法的研究和建立需要行業的推動。
相關文章:

