法規概述
2020年1月3日,國務院常務會議通過《化妝品監督管理條例(草案)》(下稱“新條例”)。2020年6月29日,新條例正式公佈,並於2021年1月1日起正式實施,要求在中華人民共和國境內從事化妝品生產經營活動及其監督管理,應該遵守新條例。
行政許可批件/備案憑證是產品進口、上市的重要審核依據,化妝品註冊/備案是其成功銷售前不可或缺的步驟。
化妝品定義
化妝品是指以塗擦、噴灑或者其他類似方法,施用於皮膚、毛髮、指甲、口唇等人體表面,以清潔、保護、美化、修飾為目的的日用化學工業產品。
化妝品的分類
根據風險程度,化妝品可劃分為特殊化妝品和普通化妝品。用於染髮、燙髮、祛斑美白、防曬、防脫髮的化妝品以及宣稱新功效的化妝品為特殊化妝品。
化妝品最後一道接觸內容物的工序在境內完成的為國產產品,在境外完成的為進口產品,在中國臺灣、香港和澳門地區完成的參照進口產品管理。進口化妝品需指定我國境內的企業法人作為境內責任人(RP)。
中國大陸化妝品監管模式
產品類型 | 特殊化妝品 | 普通化妝品 |
上市前 | 註冊 | 備案 |
申報主體 | 註冊人(國產) 境内責任人(進口) | 備案人(國產) 境内責任人(進口) |
審核機構 | 國家藥監局(國產/進口) | 國家/省藥監局(進口) 市區級藥監局(國產) |
上市後 | 延續註冊 (註冊證有效期5年) | 提交年報 |
中國大陸化妝品成品註冊/備案流程
特殊化妝品註冊週期在12-16個月,通過境內責任人RP授權、許可權開通、檢測、卷宗整理、形式審查、技術審核的流程獲取註冊證。
普通化妝品備案週期在4-6個月,通過境內責任人RP授權、許可權開通、檢測、卷宗整理、線上提交完成備案。
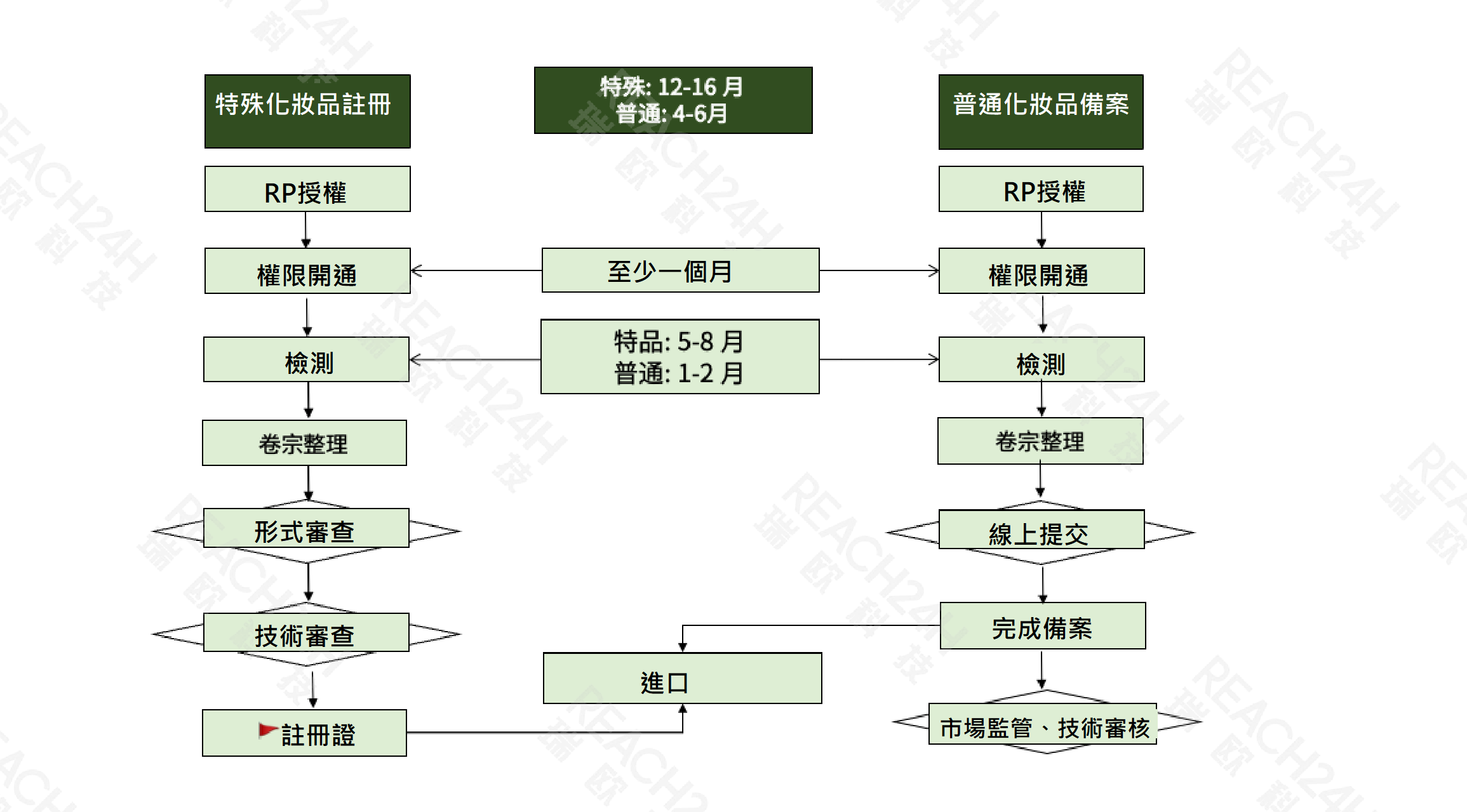
中國化妝品成品申報流程
中國大陸化妝品相關監管部門
國家藥品監督管理局(NMPA):組織實施化妝品和化妝品新原料的註冊備案工作,開展現場檢查和上市後監管,特殊化妝品上市前需要獲得國家藥監局的審批許可
中國食品藥品檢定研究院(NIFD):承擔化妝品的技術審評工作和技術核查工作,負責制修訂相關的技術規範、技術要求和檢驗方法
各省級藥品監督管理局:負責各省化妝品的生產與上市後監管,普通化妝品向省級藥品監督管理局備案(針對已下放省份)
海關:進出口清關檢驗檢疫
市場監督管理局:營業執照申請、商標申請、廣告宣傳監管
中國大陸化妝品註冊備案所需材料
註冊人/備案人資訊表
品質管制體系概述表
不良反應檢測和評價體系概述
生產企業資訊表
品質安全負責人簡歷
生產規範證明資料
產品配方
產品包裝(含標籤和產品說明書)
產品檢驗報告
產品名稱資訊
產品執行的標準(包括生產工藝簡述、成品質控措施等)
產品品質安全控制要求
產品安全評估報告
自由銷售證明(Certificate of Free Sale, CFS)
委託加工協定(如存在委託情況)
功效宣稱評價
可能有助於行政許可或備案的其他資料
樣品
我們的服務
中國大陸化妝品成品註冊備案
中國大陸化妝品配方標籤審核
中國大陸化妝品安全評估
中國大陸化妝品功效評價
我們的優勢
獨立的法規資訊平臺提供即時法規追蹤、深度解讀及專業資料庫支援
豐富的全球合作資源:政府官方、行業協會、實驗機構等
服務全球超過1000+家化妝品企業,包括眾多全球500強企業
全球分支機搆部署、多語言服務能力,具備國際化高效服務能力


